Home | Projects | CPGE | My carbon footprint
Préface : les molécules sont visualisés sous format SMILES numérique
Abréviations
- Rdt -> Rendement
-> phase - fonc -> fonctionnel
- grp -> groupe
-> proton ou particule - nrj -> énergie
- fav cin/
-> favorisé thermodynamiquement ou cinétiquement - RO -> Réacteur Ouvert
-> même
Générale :
-> néglige termes ds de type ~ puis vérifie hypothèse avec valeur trouvée
Noms et tableau:
- 2ieme ligne -> Li, Be, B, C, N, O, F, Ne = Lili Becta Bien Chez Notre Oncle Fernand-Nestor
- 3ieme ligne -> Na, Mg, Al, Si, P, S, Cl, Ar= Napoléon Mangea Allégrement Six Poulets Sans Claquer d’Argon
- Mon éléphant a des pâtes bleues -> methane, ethane, propane, butane, pentane, hexane, heptane, octane, nonane
- CIP -> Cahn, Ingold, Prelog
- VESPR -> AX5 bipyramide trig AX4 tetrahédrique, AX3 trigonal plan, AX2 lin, AX2E1/AX2E2 coudée, AX3E1 trig pyramidale (nom = nb faces)
- 400-800nm -> Very Big Geese Yeet Our Rubbish = Violet Blue Green Yellow Orange Red
- Utilisation atomique -> M(prod)/sum(M(réac))
- methanal -> H2C=O
Spectro IR
- C=C ->
(nb d'onde), = 5-6ppm (déblindage sans unité) - C=O ->
- C=O et C=C conjugué -> affaibli C=O donc blinde H de
car moins situés sur oxygène diminue -> liason moins forte d'apres Hooke eg OM L vacante avec interactions AL internes qui se remplie lors liason M
RMN
- Principe RMN -> Aimant excite état spin
+1/2 à -1/2 avec , puis passe en récepteur mesurant de la désexcitation : FFT donne - Déplacement
appareil cste -> , réf avec TMS tétraméthylsilane ou avec solvant - Déplacement
appareil B cste -> - Blindé -> "= bouclier", car noyau protégé par plus
=> diminue car moins d'effet - Déblindé -> "=retirer bouclier", appauvri
=> augemente ( attire vers lui => déblindé) - un
(ou groupe de eq) -> n voisins => le signal correspondant présentera (n+1) pics (doublet de doublets si deux non eq...?) © eq -> plan sym/libre rot => eq => - grp de
proche d’atomes électronégatifs, augemente = déblindés. - Les
liés atomes avec liaisons doubles (C=C ou C=O) -> très déblindés - Hauteur courbe d’intégration -> proportionnelle au nombre de
eq associés au signal - États spin -> en nb
, si spin I=0, sinon - Lèver la dégénérescence -> mettre particule ds
(effet Zeeman) car moments mag de spin s'alignent parallèle/antipara en f° de la charge, en tournant autour de l'axe (= toupie) -> résultante moments mag de spins - Vecteur moment mag ->
donne formule fonda RMN - Excès de magnétisation -> si
plus particules w/ même spin - fr travail ->
avec la cste gyromag, il faut choisir et tels qu'on se trouve à une fr de résonance des - Excitation réel -> on envoie une gamme de fr car
n'ont pas les environments, mais on pourra négliger cela en vue largeur du spectre reçu - Résolution de l'appareil ->
avec B car plus grande fluctuation de l'énergie de d'etat des atomes - Excitation résonant -> passage de diff états de spin e.g. -1/2 à 1/2 puis émission lumière
- Free induction decay -> solénoïde w/ AC ds lequel sont noyaux
- Temps relaxat° -> après excitat°, il faut attendre 5-6 fois
pr revenir à relaxat° longitudinale -> lié voisins noyaux, pr donne infos mvmt mol relax transversale -> dépends homogénéité de : signal de largeur sur graphe, dépendant des fr, - Temps relax
-> - Plaques shim -> permettent homog
- Spinner -> tourne tube essaie pr corriger inhomog locales, permet voir singulet/doublet etc
- Champs écran
-> format° champ diamag empêche résonance => + amp - Fréquence de Larmor -> réf en rot à
- Effet de toit -> tendance pour deux groupes de pics de même hauteur a prendre la forme d'un toit en se rapprochant
- Sys AX (2
) -> 2 doublets de pics de hauteur et fines, lorsque - Sys AM -> 2 doublets pics plus proches, petites et de legeremen diff tailles, éloignés mtn de
- Sys AB -> 2 doublets de hauteurs très différents selon effet toit
- Sys A2 -> Isochronie, mtn
pic (cas H eq) - Sys AX2 -> 3 interactions spin-spin diff au niveau du
- Si on irradie constament à
de l'hydrogène => ils s'excitent/desexcitent en permanence et donc on peut ignorer leur couplage avec les autres espèces (car ils sont de synchronisés à la différence de lorsqu'on fait une irradiation instantanée)
Effets des grps en RMN
- Effet 1%
-> couplent créent mini pics autour de la base du signal vrai - Effet VdV ->
- Effet Deutérium D -> aucun signal RMN, alcool w/
peut se deuterer en présence et disparaître du spectre => il faut ajouter de l'eau pr reprot - Règle Karplus ->
- Fluor 19 -> suit règle Karplus
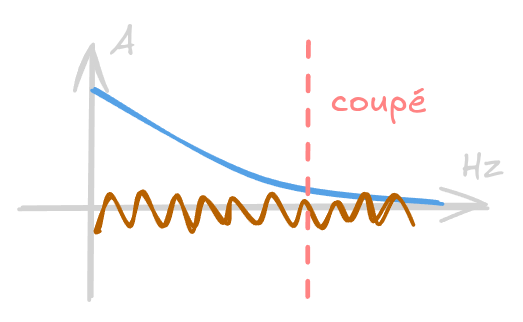
- Rapport signal/bruit ->
si on coupe haute fr => mais perds proportionnalité nb noyaux/
Cinétique (
- Vit vol R° ->
à vol cste (x avancement vol) - Vit disp A ->
- Temps 1/2 R° ->
, R° fini - Ordre R° ->
=> - Ordre 0/1/2 ->
/ / (dim k varie) - AECD -> actes successifs avec
(énergie d'activat° important) => - AEQS ->
- Pre-equilibre rapide -> utile pr IR peu réactifs qd
AEQS, eq atteint entre prod/réactif lorsque alors donc Qr=K° - Réaction par stades -> chaque IR formé est consommé dans l'étape suivante et n'est pas régénéré
- Réaction en chaîne ->
IR formé, consommé puis reformé: 1) amorçage : création 1ier IR 2) propagation : transfo reacts en prods et conso IR 3) terminaison : conso derniers IR - Michaelis-Menten ->
et alors pre-eq rapide: ⇔ - Constante MM ->
Interactions:
-> -> -> - Puissance effets stabiliseurs -> méso donneur > inductif donneur/attracteur (comparer
, et alkyl tjrs donneur) - Keesom -> some of deez nuts : deez = deux polaire
- Debye -> Demie : 1 polaire, 1 polarisable
- London -> apolitical : 2 apolaire
- van Der Waals c la somme des 3
- Puissance VdV -> Keesom > Debye > London et VdV=
- Insaturations ->
Ah je sature! D(eux)(carb)onne moi(ns) un 2eme ou 3eme demi verre!
Attaques:
-> ordre 2, 1 étape, sensible encombrement => regio, inversion Walden -> ordre 1, 2 étapes, IR plan => mél final racémique -> grp nucleofuge sur et H sur subit atk base, crée C=C, necessite chauffage: regioselective si plusieurs avec -> -elim ordre 1, 2 etapes (et inversement): suit Vant Hoff, et n'est possible que en position décalé anti, stéréo si possède 1 H, E2 suit Van't Hoff -> ECD monomoléculaire, cb= base conjuguée (permet départ grp partant) -> - Loi de van't Hoff -> pr étape ele, ordres partiels = nb stœchiométriques.
Halogenoalcanes
- Zaïtsev -> lors déshydrohalogénation (
-elim, E2...), alcène maj est celui + stable selon : 1) db liason conj 2) substitution alkyles (grps electro donneurs) 3) (E) +stable (Z) - Réactivité
-> © - Réactivité E ->
- Compétition subs/elim -> si reactif à la fois Nu et base:
et fav elim
Chimie quantique
- indice liason ->
: 1/2ice L-iALson - Liant car liées même couleur
- Pauli -> Quanti(que) : nombres
- Klechkowski -> Check how it's (filled)
- Hund -> (Mini)mund : spin para pour énergie MINimale
- Nvx énergie atome d'Hydrogène ->
- Symétries -> sigma autour de l'ax e, π sinon
- nrj OM liant/antiliant ->
- Loi Hooke ->
liason = ressort, nb onde diminue => liaison - forte - Nbx Quant ->
, , , (pas de 1 même si s pas entier) - Terme spectroscopique -> Sober Physicists Don't Find Giraffes Hidden In the Kitchen (s,p,d,f,g,h,i,k)
Orbitales frontalières :
- Approx Fukui -> HO énergie+ haute reagit BV énergie+ basse sous CC
- Recouvrement axial > latéral
OXYDORÉDUCTION:
- Règle
-> Meilleur ox réagit avec meilleur red - Order of redox -> always Ox Red (couples, échelle avec flèche Ox | Red, Nernst Ox/Red
, Ox augemente haut pot, sur graphique sens horaire augemente -> plus grand plus grand: écart pour n=1 on considère totale (domaines prédominance disjoint) -> inverse, écart grand => quasi nulle - Échelle pot. nombre d'oxydation -> alcanes < OH, C=C, RX < carbonyles, diols < acide carbox
- Ampholyte redox -> participe 2 couples
- Dismutation -> (Deez = deux du meme) réaction ampho sur lui même VS médiamutation réaction inverse
- Enthalpie libre electronique -> Dans sens RÉDUCTION
or donc - Nernst réel ->
- Nernst opérationel ->
- ESH ->
, , 1 bar - Relation charge-intensité ->
RÉDUCTEURS:
-> (red) ion tétrathionate/ thiosulfatethiosulfate
OXYDANTS:
/ -> (ox) ion dichromate/chrome / -> (ox) ion permanganate/manganèse / -> dichlore (ox PUISSANT) / -> (ox) ion hypochlorite / -> (ox) peroxyde d'hydrogène
Potentiels E°
/ -> 0V / -> 1,23V
ACIDE-BASE:
-> pour n'importe quel espèce - Order of acide base -> always Base Acide except couple AH/A- (echelle,
, , Henderson - pKa faible ->
grand => acide fort - Base (acide) Lewis -> donneur (accepteur) électron
- Base (acide) Bronsted -> donneur (accepteur) proton
- Relation ph -> pH = 14 + log(OH-)=-log(H3O+)= 14-pOH
- Solution tampon -> contient acide/base faibles conjugués => Henderson
car on se situe à 1/2 équivalence (conc egaux): peut etre préparé avec base forte + acide faible ou inversement
RÉACTIVITÉ PKA W/ BASES DE AH/A-:
- pkA
anhydre -> -7 - pkA
et -> 0 - pkA Acide aminé (cas particulier) -> 2
- pkA Acide carbox
-> 4,5 - pkA
ou -> 10 - pkA
et -> 16 - pKA énolate -> 20
- pKA alcyne vraie -> 25
- pKA
amidure de sodium -> 33 - pkA
inclu LDA -> 35 - pkA grignard -> 50
- pkA
et inclu hydrures alcalins (NaH, KH, LiH avec couple ) (purement basiques !) -> 50 - pkA Buli/nBuli -> 50
[Li+].CC(C)[N-]C(C)C
- 50 nBuli (=Buli)
[Li]CCC[CH2]
- Pour deprotonner base doit -> avoir pkA bien plus élevé
base super forte (organolithien) - Na(s) -> R° redox
E-pH :
- Diag E-pH -> front verticale <=> même no, perte/gain
ou , front horiz <=> no donc , oblique les deux - Convent° front usuel -> Solide/sol :
, X/gaz : , sol/sol : - Convent° front espèces ->
et - Convent° atomique -> égalité conc au même nb d'atomes eg
jd - Méthode E-pH -> tableau no, det front vert avec eq dissolut° + LAM
Solubilité
- Ks -> vers la solution
- Solubilité -> masse max soluté ds 1 L solvant
- Compétit° précipit° d'ions -> lim sat atteint qd
avec même et stoech - Milieu acide dilué évite précipitation
À Reclarifier
Amine en complexation amène 3 H
NO nitrosyle
Cyano CN
Électrodes : pH: intégrée verre
Potentiel: calomel
Complexation 1:
de coordinat° -> édifice polyat : centre métallique M (ALewis accepte , svnt bloc d) coordiné w/ anions/mol (BLewis, atk avec db liiant) = ligands L, stéréochimie - Métal de transit° -> sous couche d
remplie - L monodentate -> liason L-M assuré
! at de L ( plusieurs sites => poly dent=sites) - Noms
-> hydruro/oxo ( ), fluoro..., cyano, thiocyanato ( ), oxalato - Nom L neutre ->
méthanamine, 1,2-diaminoéthane, ethylène, triphénylphosphine - L particuliers ->
aqua, ammine, carbonyle, nitrosyle - Nom
-> 1) ion si chargé 2) nb L (mono, di, tri, tétra) 3) nature L ordre alpha 4) nom M (suivi -ate si anion) puis no(M) "(+IV)" - Coordinace (nb sites coordinat°) -> nb de sites de L liés M
- no(M) -> faculté M accepter
, dissociat° db vont sur ligands + , tjrs > 0 - NEV(M) ->
liasons L-M attention compte que couche d pas s,p!!! - Eq
-> - Eq
ation -> - Cste format° ->
, Beta make some complexes (breaking bad) - pKd ->
- Diag prédom -> gradué en
: pL> => et inversement (L grd = ML grd=> pL petit) - Diag distrib ->
% ou M = f° pL, intersect° 2 pL=pKd/n, - Effet chelate -> augmentat° de la stabilité
avec ligands polydentates (compétit° avec monodentates) (à même indice de coord de M) (car nb entités augemente => => donc diminue fav sens directe) - EDTA ->
- Règle du gamma -> s'applique sur pKd (sinon diag prédom)
complique -> A/B avec ligands A/B, redox avec métaux qui se , les précipitations, et il y a svnt compétition entre plusieurs - Cste format° successive ->
Complexation et orbitales 2:
- liason M-L -> liason de coordinat° = cov partiellement ionique
- nvx E
-> M -electroneg possède généralement orbitales + hautes en energie - OA d -> dxy/dyz/dxz/dx2-y2 ont quatres lobes ds plan décrit, dz2 a deux lobes et un cercle au milieu sur oz, attention axe inter nucléaire sur important
- choix site liason L -> liason avec atome sur lequel HO est + localisé : cet OM fait donat°
ou (peut aussi être \ accepteur avec OMs vacantes interagissent OA d) - donat° -> se fait tjrs vers M, sinon parle de rétrodonat°
- rétrodonat° -> renforce liason avec format° OM liante
-> liason M-dérivée éthylénique ou sys (les OM) même direct° metal (sens dz2) (on admet compris entre E OF de L) : (HO) => donat°, (BV) => rétrodonat°
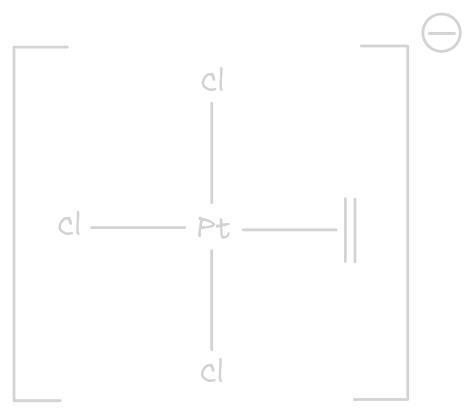
- Peut avoir C=C lié en sys pi
- Longeur liason augmente -> moins forte avec occupat° du a rétrodonat°
comme cat -> modifient densité elec ds molécule orga (donat°/retrodonat°), ou repositionnent optimalement réactifs - cycle cat -> 1) introduct° précat/précurseur (pas regénéré) qu'on transforme en cat situé sur le cycle 2) R°s avec elim prod, ajout reactifs (écrire no(M) chaque étape pr identifier R°)
- associat°/diss
-> classique © - ech/subs ligands -> remplacement L
- addit° ox/ elim red (AO, ER) -> XY se scinde en deux
: sens dir fav faible no, indir ceux fort no - Syn grignard AO -> RX+Mg(s)=R-Mg-X no(Mg) passe de 0 à
- insert° -> ligand A=B insaturé s'insère sur ML sans variat° no : type (1,1) obtiens
et type (1,2) obtiens : une étape de complexat° puis une migrat° ° (1,2) et (1,1) méca -> (1,2)
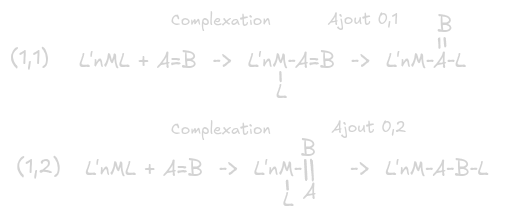
- élim non reductrice = désinsert° -> R° inverse insert° :
-elim pr (1,1) négligeable, -elim (1,2) - Sur cycle ->
AO = ER, flèche entre et sort <=> échange, peut avoir plusieurs R° une étape - Polymères se fabriquent sur cycles
Thermodynamique:
- Ext VS Int var -> Extensive massive black hole (mass)
- Carré thermo borne -> Good physicists have studied under very fine teachers
- Enthalpie -> H=U+PV
- R° endo (exo)->
(<0) => - Enthalpie Libre -> G=H-UV=H-TS et
- Enthalpie libre std ->
- Petite var H -> dH=Qp=CpdT Des hâches c'est pêté (isoT,P)
- Enthalpie molaire ->
J/mol - Sens évolution spontanée ->
- Condit° eq ->
donc - Approx d'Ellingham ->
indep T - Vant Hoff ->
demo avec d' partielles G/T par rapport T puis swartz, permet faire integrat° - Affinité chimique -> A=-
donne crit evol A.d >0
R1, R2, R3
-> pr 1/2 eq ds sens réduction ( charge par mol), eq globale donc - Condit° eq ->
=> - Pile Daniell -> -R1|Ox1||pont salin||Ox2|R2|+, convet°
, et à courant =0, alors (idem en °) - Coef T pile ->
- Vit globale surf. ->
= , car et nb éch en dt - Comparer
, -> => i>0 => ox - Montage 3 électrodes -> Viagra rêve ton cul, CE inerte, ref pot connue
- Pôle + -> cathode <=> réduct°
- Qtot -> peut fournir A.h
- Moles d'e ech ->
- Énergie cons électrolyse ->
-> qd deux Nernst egaux, - Surpot seuil ->
, f° de T, , electrode, couple - Loin Eeq -> transfert mat limitant: convect° par mvmt solvant, sinon diffusion vers zones - concentrés => pallier (si espèce dissoute, pas si électrode/solvant
couple) - Courant lim diffus° ->
avec une cste de diffusion - Domaine inertie electrochim solvant ->
2 barrières infranchissables = murs du solvant (solvant agit redox dehors) - i-E : pH ++ -> décalage gauche courbes
- Vagues successives ->
- Potentiel mixte ->
amp max => fav cin - Upile ->
= - Électrolyse -> on impose w/ générateur
- Rdt faradique ->
- Cémentat° -> ajout poudre métal pr faire précipiter impuretés
- Accumulateur electrochim -> gén/récepteur
Potentiels et activités chim
- Activité GP ->
- Activité soluté ds sol idéale ->
- Activité espèce s/l pur ->
- Activité sol réelle ->
-> coefficient d'activité, mesure l'écart par rapport au comportement idéal. - Relation avec le potentiel chimique ->
- Pot chim ->
= dernier terme neg sauf pr osmose - Pression osmotique->
- Eq potentiels -> à l'eq
Diag binaires:
- Thm de l'horizontal -> pr mélange idéal
, se lisent sur la courbe de rosée (pt L) et d'ébullition (pt V) respectivement - Thm moments -> chimique
(ou ), nécessite - Diag à extremum -> azéotropique (
mél idéal, mais miscibilité tot) : si homoazéotropique lors CE : 0DDL ) - Distillation -> donne résidu -volatil et distillat +volatil
- Distillation fractionnée -> colonne vigreux, plein de distillations (vapeur s'enrichie en + volatil) = zig-zag down diagramme à maximum (récupère distillat pur) ou minimum (récupère résidu pur)
- Diag miscibilité nulle -> présente courbe rosée horizontale
- Miscibilité nulle (hétéroazéotropique)-> 2
liq pure, 1 gaz, H = pt commun à à laquelle palier car 0DDL - Hydrodist -> excès eau, sert pr espèces non miscibles => CE à T cste => dist simple
- Diag avec démixtion -> miscibilité partielle A ds B ou B ds A slmt qd
et inversement (combinaison azéotrope ), diag forme arche - Diag bin isoP -> papillon horizontal coupée en bas
compo palier T CE -> hétéroazéotropique
Variance:
- Variance -> v=PI-R, PI : T,P,
et R (indep) : =1, eq ou , K°=Qr,eq (LAM) - Forme gen variance -> v=(n-k-r)+2-
avec n nb composants, k nb relat°s, r paramètres imposées, phi le nb de phases - Monovariant -> connaître 1 PI donne tt autres (idem divariant etc)
- Invariant v=0 -> coord pt triple imposées par nature
- DDL -> v'=v-C les contraintes
- Si PI
facteur d'eq -> doit le fixer pr connaître eq, eg athermique => T facteur eq - Principe de modération -> le châtelier
- Effet T sur eq -> Vant Hoff, R° endo (exo) fav T++(--)
- Effet P sur eq -> loi dalton ds Qr (idem effet compo)
Contrôles
- Cinétique -> compare stabilité IR
- Thermo -> comp stabilité produits
- Orbitalaire -> R° sur HO/BV coef max
- Charges -> charges nette maximale v.a. réagissent
Réacteurs ouverts (RO)
- Vit vol R° ->
ou dV si infinitésimal - Débit mol ->
et => - RPAC -> fermé, T et
uniformes en RS ( cons), R° liq incomp ( solvant donc ) - Rdt RPAC ->
(catho en croix) : car RS or donc et - RP ->
<=> <=> or vit vol et pr ordre 1 => et
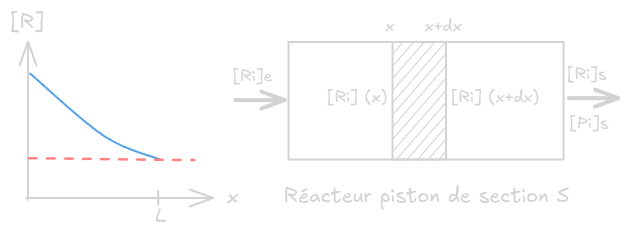
- Thermo/cin RO -> Arrhenius : T + => k + => fav cin
Composés bizarres:
- Zwitterion -> associé acide aminé ou il y a
et l'acide est deprotonné (O4)
C1=CC=C(C=C1)CC(C(=O)[O-])[NH3+]
- d' d'acides ->
= peuvent subir puis avec - Electrophilie
-> augmente avec diminution => - Réactivité pr
-> chlorure d'acyle d'acyle > anhydre d'acide > RCOOH > cétone > amide - Activation ex-situ COOH en acyle ->
, , agents chlorant dans pyridine sous - Synth anhydre d'acide -> acide carbo +
en (que pour les symétriques) - Activat° COOH in situ -> COOH et
- Activation COOH agents couplage -> DCC
- Estérification de fischer -> RC(=O)-OH+HO-R' = R-C(=O)-OR'+
, R° lente athermique et limitée, , déplacement eq DS / excès : Pour OH( , ) cat acide active C=O puis atk de OH, prototropie puis elim eau, impossible OH( ) - Synthèse esters with acyle -> RC(=O)Cl+R'-OH=RC(=O)OR' + HCl(g) rapide, quantitative et avec alchools
, mais faut pieger gaz base pyridine : OH sur acyle, elim puis A/B - Synth esters anhydre d'acide -> BnOH+CC(=O)OC(=O)C=CC(=O)Bn +CH_3COOH avec
OH sur AA, elim ion carboxylate qui va ensuite capter H de alcool : reaction sensible encombrement et pas de pyridine nécessaire - Transtérification -> transfo chaine n esters et n alcools en chaine, cat milieu acide = Fischer*n avec esters
- Synthèse différents amides -> d' acide avec Z nucléofuge +
; Primaire : + ; Secondaire : +amine tertiaire ; impossible COOH car R° A/B fav formant - Synth amides acyle/AA ->
d'azote sur puis et base récupère , produit HCl pr 1ier - Acide
-aminé -> avec sur : tous chiraux sauf si R=H - Liason peptidique avec 2 acide
-aminé -> OH et couplent donnant C1-NH-C2 et - Monomère -> morceau polymère
Réactivité d'énolates (O4):
- énol (cétol) -> alcène (cétone) avec un -OH en position vinylique (sur C=C) : en équilibre avec cétone,
trés défav (sauf si existe noyau aromatique ou C=C conjugé sur ou liasons H internes avec dicétone ou qu'il y a formation d'un noyau arom), formée sous cat acide/basique
CC(=C)O
- Ion énolate -> charge formelle sur O ou sur
, pKa 20, stabilisé par méso avec carbanion, préparé quantitativement base forte pkA>30 ou catalytiquement soude/potasse, et reaction tirera l'eq en sens directe
C(=O)[C-]([H])[H]
C(=C)[O-]
- Controle thermo/cin sur énolate -> thermo suit Zaitsev ou cin déprot C - encombré par base encombé type LDA
- R° impossible pr esters avec
car base donc saponification -> - énolate est la forme déprotonné d'un énol
- Extracteur Soxhlet
An suivi de E (O5):
- electro
C <=> diminue -> Réactivité amides < acide carbo < aldéhyde< Cl d'acyle - effets elec Z -> Cl > anhydre d'acide (-O, -CO, -R) > acide (-OH) > Ester > amide
- Bon nucleo
Z -> pKa < ion carbox < ion ester < amide < cétone - Bilan réactivité -> Cl d'acyle > anhydre d'acide > acide carbo > ester > amide
- Activat° electro
acide ex situ-> , ou crée anhydre d'acide - Activat° in situ -> protonat° O de C=O
- Agents couplage -> DCC active électro
C - Esterificat° Fischer ->
(fisherman => williamson prod eau), Dean Stark, cat acide, seulement R , prototropie - Synth esters Cl d'acyle ->
alchool puis E Cl, pyridine pr H+ ( ), rapide quant - Synth esters w/ anhydre acide -> An puis E et ion estzr
Vademécum de groupes communs:
- Toluène -> cycle 6 C conjugés 1 méthyl
CC1=CC=CC=C1
- Sulfonyle -> O=(S(-R)-R)=O
O=S(=O)(*)*
- Benzyl -> symbole Bn (eg Bn-OH alcool benzylique)
[R]-C-c1-c-c-c-c-c1
- Cy -> cyclohexyl
C1CCCCC1
- Formaldéhyde -> l'aldéhyde le + simple
- Nitro ->
- Anhydre d'acide -> deux esters partageant O centrale
CC(=O)OC(=O)C
Catalyseurs:
- Pd de Lindlar -> empoisonné va jusqu'à C=C
- Nickel de Raney -> va jusqu'à C-C
- mCPBA ->
catalytique
Collent l'alcool, hydro acide rend flacide:
- (O)Ts -> sans le reste, nucléofuge l'alcool bouge (paratoluènesulfonyle)
- (O)THP -> reste baiser (tetrahydropropane)
- (O)Bn -> reste ken (Benzyle)
- ATPS -> active O sans reste
CC1=CC=C(C=C1)S(=O)(=O)O
- LDA -> crabe H s'en va (base), Li+ et N-, moins nucléophile que n-bulli
CC(C)[N-]C(C)C
Acide base/nucleophilie:
- t-BuOK -> base forte, mauvais nucleophile
-> acide fort, sert à hydratation acide suivant Markovnikov avec attaque d'un hydrogène puis d'une molécule d'eau, régénération de
S(=O)(=O)(O)(O)
- R-NH, CN-
- NH4+ acide faible
Touchent les groupes:
- Dibal-H H- faible, réduit ester en aldehyde
[H-].CC(C)C[Al]CC(C)C
- LiAlH4, a 4 H- qui mattraquent, elle n'est pas chimio, reduit en alcoo(l), meilleur que NaBH4 (peut pas réduire esters, amides, acides carbox)
- Sarret oxyde alcool (s'arrete à l') en aldehyde,
ds pyridine - Jones: CrO3, Old Joe Crow ds H2SO4 oxyde audelà <=> dichromate de potassium
en milieu acide (tt deux toxiques): oxydent alcool en acide carbox, alcool en cétone - le MCPBA, peroxyacide commun, oxyde l'alcène, epoxyde stereogene, stereospecificité aussi est là (et regiosélectivité) (peracide attaché à chlorobenzene), (généré in situ carbox + H2O2)
C1=CC(=CC(=C1)Cl)C(=O)OO
- Ouverture epoxyde avec
ou RMgX -> SN2 atk sur C moins encombré (régio), puis hydrolyse, forme HO ou R en anti cat SN2 (stéréoselect)
C1OC1C
Transfo d'alcènes
- Markovnikov -> OH maj formé est issu carbo plus substitué par grps donneurs d'
(regio) (attention cas particulier existe mésomérie) - Effet Karash -> anti-markovnikov
- Oxydation avec
-> atk sur C de C=C le moins substitué puis atk et deprotonation donne alcool - Hydroboration ->
ds solvant base lewis qui solvate lacunes ( , THF...), syn-addit° (aucun carbocat°) anti-markovnikov (se fixe sur C - encombré donc - substitué) de sur C=C, l'autre, puis oxydé en milieu basique avec pr donner alcool. Attention le bore peut attaquer pls fois (tri-alkyl-borane) - Hydratation d'alcènes -> Rcc + H2O = ROH, CC avec excès d'eau, cat acide, suit Markovnikov, activation cc
puis eau, + rapide si subs + grps electro donneurs, attentuation grp électro attracteur avec distance
Activations:
- Protonation -> OH avec ATPS, acides forts ; cétone avec
Protections:
- R-OH -> chlorotrialkylsilane
en presence base faible type pyridine. {Ph, trialkyl} pr selectionner alcools peu encombrés
[R][Si]([R])([R])[Cl]
- Ethers benzyliques -> BnBr+NaH+R-OH=BnOR car
après que NaH déprot alcool = Williamson
Solvants:
- Base de lewis (BdL) -> sert solubiliser lacunes
- Aprotique évite trucs ©
- diéthylether -> batman: base lewis (RMgX)
CCOCC
- THF -> polaire, BdL (solvatat° RMgX), aprotique, oxacyxlopentane
C1CCOC1
- pyridine -> polaire aprot, BdL
C1=CC=NC=C1
- DMSO diméthylsulfoxyde -> polaire, aprot, BdL
S=O
REACTIONS:
- R° combustion ->
- Umpolung -> RX(dans Et2O)+Mg=RMgX mat séché etuve car R A/B H20-organomag, bain glacé, CaCl2, RX goutte a goutte eviter Wurtz, pince 3 refrig et isobare, 2 ballon, N2
- Wurtz -> RMgX+RX=RR+
- Williamson -> ROH+RX +NaOH= ROR+NaX+
his son is water bender - Williamson intra ->
= + expoxyde : plus rapide que inter - Préparation quantitative énolates w/ base forte -> NaH, LiH
- Sechage -> Sulfate de Magnésium anhydre, ajouté jusqu'à qu'on perçoit des grains de solide virevolter
- Dean Stark -> il faut que solvant orga soit moins dense que l'eau pour que ça retombe en solution avec l'appareil de Dean Stark. De plus il faut que la fraction massique en eau dans l'heteroazotrope qui se liquéfie dans le réfrigérant soit important pour justifier l'utilisation du DS.
- Acételisation -> il faut que le solvant dissous bien les espèces, créat°/destruct° cycles, activat° cétone
puis atk OH sur , régénération cat
Nomenclature générale
- Aldéhyde (Alde-hide) -> R-H suffixe -anal (pentanal), indice position tjrs 1 (pas chiffre) (-énal signifie
C=C aussi) - Cétone (Set-one -> R-R suffixe -one, préfixe oxo
- ortho (o), meto (m), para (p) -> pos 2,3,4 par rapport au carbone fonc (
)
CCC1C(O)C(=O)C(O)C(CC)C1P
- Ester (Este-rior) -> R-OR, Méthanoate (sans O et inclu Cfonc) de butyle (avec O)
- Acide carboxylique -> acide -oïque yg
- Éther-oxyde -> R-O-R', prefix oxa, base lewis
- https://www.chem.ucla.edu/~harding/IGOC/C/common_name.html
-> hydronium oxonium - Ni-tri-l -> N#CH
- Amine -> R-NH2 has less than amid -amine, présence d'amine => A/B créé
avant de pvr activer O de acide carbo etc - Amide R-(C=O)-NH2 has more than am in
- Éther-oxyde (Ethe-ror-xyde) -> R-O-R
- Hémiacétal -> alcool + aldéhyde cat
[H]C([R])(O[R])[OH]
- Hémicétal -> Idem hémiacétal mais avec un H au lieu d'un des 2 R
[R]C([R])(O[R])[OH]
- Acétal -> Diol + propanone ou 2-dimethoxy-propane et
C1COC(C)(C)O1
- Anhydride d'acide ->
CC(=O)OC(=O)C
- Cas particulier cétone -> pentan-3-one mais 2-méthylpent-3-one
Nomenclature stéréochimique
- R/S -> Rectus = dRoite, Sinister = sinistra en italien = gauche
Mécanismes réactionnels:
- Chimioselectif -> 1 grp f° privilégié
- Régioselective (Stéréosel) -> forme 1 iso const (stereoisomère) préférentiellement
- Stereospecifique -> reactifs
stereochim => prods stereochim: Diels Alder est stéréospécifique, les cis restent avec les cis, les trans restent avec les trans (ou cis donnent trans, trans donnent cis) - Postulat Hammond-> 2 états successifs ont E semblable <=> faible réorganisation moléculaire, donc R° exo (endo) => ET
reac (prod) => ET précoce (tardif) - Loi Vant Hoff pr acte ele -> ordres partielles = coefs stoech et ordre global = molécularité
-> acte ele non renversible
Caracterisation chimique:
- énantiomères -> images MP (dia ne l'est pas)
- Chiral -> C* et pas de plan de symétrie <=> non superposable image miroir plan
- Activité optique (pvr rot) -> capacité tourner lum polarisée, mesuré par polarimètre de Laurent, nulle si mélange racémique
- Loi biot ->
en degrés - diol anti -> 2 -OH pas ds plan molécule
Cristallographie
- Cristal -> solide doté structure 3D unique conférant un ordre à longue distance
- Réseau -> distribution tripériodique de nœuds
- Nœuds -> points d'ancrage d'un motif identique (équivalents par translation du réseau de
avec a,b,c une base de l'espace) ; m nb nœuds => m V ; compte pr 1 milieu, 1/2 face, 1/4 arrête, 1/8 sommet - Maille simple/primitive ->
nœuds aux sommets - Paramètres maille -> a,b,c et
, - Critères choix maille -> 1. + sym (angles
ou ) 2. - grd 3. + régulière - Coordonnée réduite ->
avec a en Armstrung => nœuds coord entiers (ou 1/2 entiers si maille multiple) - Axe/rangée réticulaire
-> droite passant par nœuds M,M' tq MM'=u.a+v.b+w.c ou u,v,w premiers entre eux (PEE) => axe principales ... - Plan réticulaire
-> eq cartésien coefs h,k,l PEE ; familles formées par valeur m ; faces cristaux sont plans réticulaires - Projection stéréographique ->
- Variété allotropique -> diff struc cristalline
- Rayon métallique (cov) (ionique) ->
+ proches (liées cov) (anion-cation) - Compacité ->
- Habitabilité (d'un site) -> rayon maximale espèce dedans
- Empilement compacte ->
sphère tangent à 6 autres ds plan, et plans décalés - Cubique centré -> chaque sommet et centre
- CFC -> cube côté a, condition contacte
, centre chaque cube côté a/2 = site tétra tq , milieu arrêtes extérieurs + centre = sites octa tq - Crystal macrovalent -> espèces liés liasons cov
- Graphite -> plans macrovalents liés VdV
- Aire hexagone -> 6x Aire triangle
HP orga:
- Coupure oxydante ->
+ réduction (Zn, Me_2S) brise liason C=C sur C plus substitué en ajoutant O sur les deux nvlles molécules